Teratogenost lijekova. Teratogeno dejstvo lekova
Opće informacije
Djelovanje teratogenih faktora ima graničnu prirodu, odnosno za svaki teratogeni faktor postoji određena granična doza teratogenog djelovanja. [ ]
Osetljivost na teratogena dejstva zavisi od faze embrionalnog razvoja: kod ljudi u fazi blastociste, izloženost nepovoljnim (uključujući teratogene) faktorima dovodi do odumiranja dela blastomera (ćelija blastociste): ako su oštećene veliki broj blastomera, embrion umire ako je oštećen relativno mali broj blastomera, dalji razvoj nije poremećen. Maksimalna osjetljivost na teratogene faktore u ljudskom embrionu javlja se 18-60. dana razvoja, odnosno perioda intenzivne ćelijsko-tkivne diferencijacije i organogeneze. Nakon ovog perioda, štetni efekti obično ne dovode do malformacija, već do nerazvijenosti ili funkcionalne nezrelosti organa fetusa.
Istorija koncepta
Teratologija je dugo privlačila ljude koji su sa zanimanjem razmatrali različite mogućnosti poremećaja i odstupanja od norme. U srednjem veku, bogati ljudi skupljali su patuljke, sijamskih blizanaca i druge osobe sa različitim očiglednim fizičkim oštećenjima.
Kasnije je uočeno da određene supstance, biljni preparati ili fizički uticaji mogu povećati učestalost deformiteta.
Posebno jaka pažnja Problem teratogenosti lijekova bio je fokusiran sredinom 20. stoljeća, nakon skandala sa tabletom za spavanje talidomidom, koji je uzrokovao evropske zemlje masivni razvojni poremećaji udova kod djece čije su majke koristile ovaj lijek tokom trudnoće, ovaj slučaj je kasnije nazvan „tragedija talidomida“ i bio je važan u formiranju sistema kontrole droga.
Krajem 20. stoljeća ispitivanje teratogenosti i mutagenosti supstanci postalo je dio prakse praćenja većine novih sintetiziranih supstanci, industrijskog otpada, kao i dugo proizvedenih velikih proizvoda kemijske industrije.
Teratogenost
Teratogenost je sposobnost fizičkih, hemijskih ili bioloških faktora da izazovu poremećaje u procesu embriogeneze, koji dovode do pojave kongenitalnih deformiteta (razvojnih abnormalnosti) kod ljudi ili životinja.
Primjena testova teratogenosti
U farmakologiji
Klasifikacija lijekova prema stepenu teratogenosti (SAD)
- Kategorija A - lijekovi sa neotkrivenim teratogenim efektima bilo u klinici ili eksperimentalno. Nijedna studija ne može u potpunosti isključiti rizik od teratogenosti.
- Kategorija B - lijekovi koji nisu imali teratogenost u eksperimentu, ali nema kliničkih podataka.
- Kategorija C - lijekovi koji imaju negativan učinak na fetus u eksperimentu, ali nema adekvatne kliničke kontrole.
- Kategorija D - lijekovi koji imaju teratogeni učinak, ali potreba za njihovom upotrebom nadmašuje potencijalni rizik od oštećenja fetusa. Ovi lijekovi se propisuju iz zdravstvenih razloga. Žena treba da bude obaveštena moguće posljedice za fetus.
- Kategorija X - lijekovi dokazane teratogenosti u eksperimentima i klinikama. Kontraindikovana tokom trudnoće.
U ekologiji
Ispitivanja teratogenosti dio su programa istraživanja tvari kako bi se razjasnila njihova potencijalna opasnost za ljude i okoliš.
Američki koledž za akušerstvo i ginekologiju. Teratologija. Smjernice br. 236, april 1997.
S engleskog preveo doktor S.V. Meglei, Porodilište, Benderi.
Supstance koje nisu prijavljene kao teratogeni(kontakt sa ovim sredstvom nije rezultirao teratogenim efektima).
Lijekovi i hemijske supstance.
Acetaminophen Acyclovir Antiemetici (fenotiazini, trimetabenzamidi...). Antihistaminici Aspartam Aspirin Kofein Lak za kosu Marihuana Metronidazol Manji sredstva za smirenje Profesionalni hemijski agensi Oralni kontraceptivi Pesticidi Trimetoprim - sulfametoksazol Vaginalni spermicidi Zidovuline
Infekcije
Virus Herpes simplex tip 2 Parvovirus B19
Fizički agenti
Elektromagnetna polja sa TV i kompjuterskih monitora Pregrijavanje
Teratogeni.
Lijek
Efekat
Komentar
Alkohol
Kašnjenje u razvoju prije i poslije rođenja, kašnjenje mentalni razvoj, mikrocefalija, nerazvijenost struktura lica sa formiranjem karakteristike alkoholičarka, bubrežne i srčane mane, mnogo različitih velikih i malih mana.
Nedostatak u ishrani, pušenje i upotreba droga pogoršavaju stanje fetusa. Rizik od uzimanja 1 do 2 doze dnevno nije dobro utvrđen, ali može uzrokovati blagi gubitak težine. Kod žena koje su pile 6 pića dnevno, 40% fetusa imalo je alkoholni sindrom.
Androgeni i derivati testosterona (Danazol).
Virilizacija kod djevojčica i prerazvijenost genitalije dječaka.
Učinak ovisi o dozi i fazi embriogeneze. Do 9 nedelja gestacije, povećanje malih usana. Povećanje klitorisa u bilo kojoj fazi. Rizik od jednokratne upotrebe je minimalan.
Inhibitori enzima koji konvertuje angiotenzin (kaptopril).
Bubrežna tubularna displazija, oligohidramnion, zatajenje bubrega, nedovoljna osifikacija lobanje, IUGR.
Rizik od oštećenja je 30%, povećava se upotrebom u 2. i 3. trimestru, što dovodi do intrauterine hipotenzije, smanjenog bubrežnog protoka krvi u fetusu i zatajenja bubrega.
Derivati kumarina (varfarin)
Hipoplazija nosa i epifiza kostiju; kratke ruke s kratkim falangama; oftalmološke malformacije; ZVRP; patologija centralnog nervnog sistema i kičme
Rizik od grubog defekta je 15 – 25% kada se koristi u prvom trimestru (inhibira vitamin K). Nakon prvog tromjesečja može dovesti do spontanog pobačaja, propuštenog pobačaja, patologije centralnog nervnog sistema, abrupcije placente i krvarenja u fetusu ili novorođenčetu.
Karbamazepin
Defekti neuralna cijev, manji defekti lobanje i lica, mikrocefalija, FGR, mentalna retardacija.
Rizik od defekta neuralne cijevi (obično limbosakralnog) je 1-2% kada se koristi samo jedan lijek u prvom tromjesečju, a povećava se kada se koristi s drugim antiepileptičkim lijekovima.
Antagonisti folne kiseline (metotreksat, aminopterin)
Povećan je rizik od spontanih pobačaja i raznih anomalija.
Ovi lijekovi su kontraindicirani za liječenje psorijaze tokom trudnoće i koriste se s velikim oprezom u liječenju raka. Citotoksični lijekovi su potencijalno teratogeni. Efekti aminopterina su dokumentovani. Antagonisti folne kiseline, kada se koriste u prvom tromjesečju, uzrokuju deformitete kod 30% preživjelih fetusa.
Intestinalna atrezija, urođeni defekti srca, lica i genitourinarnog trakta, mikrocefalija, IUGR, cerebralni infarkt.
Rizik može biti pojačan drugim faktorima. Komplikacije za trudnicu i fetus uključuju abrupciju placente i iznenadna smrt fetus
Dietilstilbestrol
Ćelijski adenokarcinom vagine i grlića materice, vaginalna adenoza, defekti cerviksa i materice, testisi kod dječaka, neplodnost kod dječaka i djevojčica.
Vaginalna adenoza se javila kod 50% žena čije su majke uzimale ovaj lijek prije 9. sedmice trudnoće. Rizik od vaginalnog adenokarcinoma je nizak. Dječaci mogu imati epididimalne ciste, hipotrofiju testisa i azoospermiju u 25% slučajeva.
Pobačaji i mrtvorođeni
Lezije centralnog nervnog sistema
Urođene srčane mane
Rizik je nizak. Lezije nisu tako izražene kao što je prethodno opisano. Kontakt u posljednjem mjesecu gestacije može uzrokovati toksično oštećenje štitne žlijezde, bubrega i neuromišićnog sistema.
organska živa (arsen)
Cerebralna atrofija, mentalna retardacija, spastičnost, sljepoća.
Može biti oštećenje mozga i nakon kontakta u trećem trimestru. To uključuje kontakt s ribom i žitaricama kontaminiranim arsenom.
FGR, mentalna retardacija, mikrocefalija, facijalna dismorfija, srčane mane, hipoplazija noktiju i distalnih falanga.
Sindrom se u potpunosti manifestira kod manje od 10% djece sa intravenskim kontaktom, ali do 30% ima blage znakove (stigme). Blaga do teška mentalna retardacija nalazi se kod djece s fizičkim manifestacijama. Učinak može ovisiti o tome da li je mutantni gen naslijeđen koji smanjuje proizvodnju epoksid hidrolaze, enzima koji je neophodan za smanjenje teratogenog fenitoin epoksida.
Streptomicin i kanamicin
Gubitak sluha, oštećenje osmog kranijalnog živca.
Nema dokaza o teratogenosti gentamicina ili vankomicina
Tetraciklin
Hipoplazija zubne cakline, prodiranje tetraciklina u kost i zube, dugotrajna žuto-smeđa promjena boje mliječnih zuba.
Oštećenje nastaje kada se koristi u drugom i trećem trimestru.
Talidomid
Bilateralna displazija ekstremiteta, anocija i mikrotija. Defekti kardiovaskularnog sistema i gastrointestinalnog trakta.
20% djece čije su majke imale kontakt s lijekom između 35 i 50 dana gestacije imalo je defekte.
Trimetadion i parametadion
Rascjep usne i nepca, srčane mane, IUGR, mikrocefalija, mentalna retardacija, karakterističan izgled lica, defekti udova, defekti oka i genitourinarni defekti.
Rizik od defekta ili s/a je 60 – 80% kada se konzumira u prvom trimestru. Sindrom uključuje obrve u obliku slova V, nisko postavljene uši, visoko gornje nepce i poremećaj rasta zuba. Lijek se ne koristi tokom trudnoće.
Valproična kiselina
Defekt neuralne cijevi (obično Spina bifida), manji defekti lica.
Defekt se javlja sa učestalošću od 1% sa kontaktom u prvom tromjesečju, prije zatvaranja neuralne cijevi.
Vitamin A i njegovi derivati (izotretinoin, etretinat, retinoidi).
Pobačaji, mikrotija, defekti centralnog nervnog sistema, ageneza timusa, kardiovaskularni defekti, defekti lobanje, mikroftalmija, rascep usne i nepca, mentalna retardacija.
Kontakt sa izotrentinoinom prije trudnoće nije opasan, jer se lijek ne zadržava u tijelu.
Etretinat ima dugo poluvrijeme, tako da se efekti mogu javiti dugo nakon prestanka uzimanja lijeka. Rizik od lokalne primjene nije poznat.
U slučaju akutne infekcije - fetalni hidrops: u slučaju srednje težine - otkrivaju se defekti kože, zuba i kostiju.
Liječenje penicilinom je efikasno. Opseg oštećenja zavisi od trajanja infekcije. Oštećenje je teže ako infekcija traje duže od 20 sedmica trudnoće. Neophodan je i pregled za druge venske bolesti.
Toksoplazmoza
Moguća su oštećenja bilo kojeg organa i sistema, ali češće centralnog nervnog sistema: mikrocefalija, hidrocefalus, kalcifikacije u mozgu. Koreoretinitis je veoma čest. Ozbiljnost lezije ovisi o trajanju infekcije.
Rijetko se javlja u trudnoći (0,10-00,5%): primarna infekcija tokom trudnoće je neophodna da bi zahvatila fetus. Toxoplasma gondii se prenosi na ljude putem sirovog mesa ili mačjeg izmeta. U prvom tromjesečju rizik od oštećenja ploda je 9%, au trećem – 59%. A težina manifestacije kod trudnice je izraženija u prvom tromjesečju nego u trećem. Liječenje: pirimetamin, sulfadiazin, spiramicin.
Citomegalovirus
Hidrocefalus, mikrocefalija, koreoretinitis, cerebralne kalcifikacije, simetrična IUGR, mikroftalmija, oštećenje cerebralnih konvolucija, mentalna retardacija, gluvoća.
Najčešća intravenska infekcija. IV infekcija je 40% nakon prve infekcije i 14% nakon egzacerbacije infekcije. Od zaraženih plodova, navedeni fizički nedostaci javljaju se u 20% nakon prve infekcije i 8% nakon sekundarne infekcije. Ne postoji efikasna terapija.
Rubela
Mikrocefalija, mentalna retardacija, katarakta, gluvoća, srčane mane, m.b. zahvaćeni su svi organi.
Stopa malformacija je 50% kada se zarazi u prvom tromjesečju. Stopa oštećenja pada na 6% do sredine trudnoće. Radi prevencije obavezna je imunizacija djece i netrudnih odraslih osoba. Vakcina se ne preporučuje tokom trudnoće, ali nema izvještaja o živom atenuiranom virusu rubeole koji uzrokuje malformacije.
Varicella zoster
Može zahvatiti sve organe (ožiljci na koži, koreoretinitis, katarakta, mikrocefalija, hipoplazija kostiju šaka i stopala, atrofija mišića).
Rizik od kongenitalne infekcije je nizak, oko 2-3%, a javlja se između 7. i 21. sedmice gestacije. Imunoglobulin protiv Varicella zoster daje se novorođenčadi koja su bila u kontaktu tokom poslednjih 4 do 7 dana trudnoće.
Radijacija
Mikrocefalija, mentalna retardacija
Medicinsko dijagnostičko zračenje manje od 0,05 Gy nema teratogeno dejstvo na fetus (doza zračenja je 0,01 Gy ili manje; kod IV urografije 0,0041 Gy).
MINISTARSTVO PROSVETE I NAUKE RF
SAVEZNA DRŽAVNA OBRAZOVNA USTANOVA VISOKOG STRUČNOG OBRAZOVANJA
"VORONJEŽ DRŽAVNI UNIVERZITET"
Zavod za biofiziku i biotehnologiju
Esej
na temu: Teratogeno djelovanje lijekova
Uvod
Teratogeno dejstvo (od grč. τερατος « čudovište, čudovište, deformitet") - kršenje embrionalnog razvoja pod utjecajem teratogenih faktora - nekih fizičkih, kemijskih (uključujući lijekove) i bioloških agensa (na primjer, viruse) s pojavom morfoloških abnormalnosti i razvojnih defekata. Teratologija je nauka koja proučava kongenitalnih deformiteta pojedinačni organi i cijeli organizmi u biljnom i životinjskom carstvu. Utvrđeno je da glavni uzroci smrti za dvije trećine djece nastaju u embrionalnom periodu razvoja, odnosno tokom prvog mjeseca života nakon rođenja. Treba napomenuti da su uzroci kongenitalnih malformacija izuzetno raznoliki, a etiologija većine njih još uvijek nije pouzdano proučena. Poznato je, na primjer, da jedno hemijsko jedinjenje (tvar) koje u jednoj trudnoći štetno djeluje na fetus može biti potpuno bezopasno u drugim, ili uzrokovati razne urođene malformacije, ili ne štetno djelovati u sledeća trudnoća od iste žene. Trenutno nema sumnje da su urođene malformacije uzrokovane djelovanjem poznatih hemijski faktori, najvjerovatnije, u općoj listi uzroka kongenitalnih malformacija čine samo 1-2% od ukupnog broja svih kongenitalnih malformacija u datoj populaciji. Istovremeno, Wilson je procijenio da je odgovornost ovih supstanci u njihovoj sposobnosti da izazovu kongenitalne malformacije mnogo veća - na 4-7%. Sa ovim se možemo složiti, budući da je poslednjih godina značajno povećana upotreba hemijskih sredstava u kućnoj hemiji, industriji, medicini itd. Dakle, nesumnjivo je da je jedan od primarnih zadataka savremene teratologije identifikacija i proučavanje potencijalno opasnih hemikalija, uključujući i lekove koji mogu štetno uticati na razvoj fetusa i trudnice, kao i na razvoj bolesti. metode za smanjenje rizika od pojave kongenitalnih malformacija. Analiza uzroka kongenitalnih maligniteta kod ljudi i životinja je razočaravajuća jer u etiologiji kongenitalnih malformacija dominira kategorija tzv. nepoznati faktori .
Trenutno je poznato da samo 19 glavnih lijekova i grupa lijekova srodnih njihovim derivatima, kao i dva hemijska elementa, imaju bezuslovni teratogeni potencijal za ljude. Kod laboratorijskih životinja, za razliku od ljudi, broj potencijalnih teratogena raste na najmanje 800. Zašto ova razlika postoji nije sasvim jasno, iako postoje određeni naučni kriterijumi koji objašnjavaju značaj ovog fenomena. 1. Istorijat koncepta
Teratologija je dugo privlačila ljude koji su sa zanimanjem promatrali razne varijante poremećaja i odstupanja od norme. U srednjem vijeku, bogati ljudi skupljali su patuljke, sijamske blizance i druge ljude s različitim očiglednim fizičkim nedostacima. Kasnije je uočeno da određene supstance, biljni preparati ili fizički uticaji mogu povećati učestalost deformiteta. Posebno jaka pažnja na problem teratogenosti lijekova bila je usmjerena sredinom 20. stoljeća, nakon skandala sa tabletom za spavanje talidomidom, koja je u evropskim zemljama izazvala masivne smetnje u razvoju udova kod djece čije su majke koristile ovaj lijek tokom trudnoće. Ovaj slučaj je kasnije nazvan “tragedija talidomida” i bio je od velike važnosti u formiranju sistema kontrole droga. Defekti u razvoju su razvojne anomalije, skup odstupanja od normalne strukture tijela koja nastaju tokom procesa intrauterinog ili, rjeđe, postnatalnog razvoja. Treba ih razlikovati od ekstremnih varijanti norme. Defekti u razvoju nastaju pod uticajem različitih unutrašnjih faktora (naslednost, hormonalni poremećaji, biološka inferiornost zametnih ćelija itd.) i spoljašnji (jonizujuće zračenje, virusna infekcija, nedostatak kiseonika, izloženost određenim hemikalijama, amnionske trake, itd.) faktori. Od druge polovine 20. vijeka dolazi do značajnog porasta razvojnih nedostataka, posebno u razvijenim zemljama. 2. Osobine upotrebe lijekova tokom trudnoće
Upotreba lijekova može doprinijeti komplikacijama trudnoće kao što su: spontani pobačaj; prijevremeno rođenje; mrtvorođenost; cerebralna paraliza; mentalna retardacija ili poremećaji ponašanja itd. Lijekovi koji ne uzrokuju organska oštećenja fetusa mogu doprinijeti razvoju alergijskih reakcija kod fetusa. Osim toga, negativni efekti lijekova mogu se pojaviti tek nakon rođenja djeteta ili kasnije. Često prateće bolesti tokom trudnoće štetno utiču na fetus, što zahteva upotrebu različitih lekova. Trudnicama se propisuju i različiti lijekovi u svrhu specifičnog terapijskog djelovanja na fetus. U ovim slučajevima, prije svega, procjenjuje se odnos koristi i štete od uzimanja određenih lijekova i oni se propisuju samo ako postoji vjerovatnoća terapeutski efekat jer majka nadmašuje rizik od razvoja neželjenih efekata na fetus. Obično se propisuju samo oni lijekovi za koje već postoji iskustvo njihove raširene primjene tokom trudnoće. Nemoguće je sastaviti tačnu listu sigurnih lijekova. Može se samo pretpostaviti da postoje manje-više sigurni lijekovi, ali se njihova bezopasnost nikada ne može u potpunosti isključiti. Do 10-12 sedmice trudnoće dolazi do formiranja svih organa i sistema u fetusu. U ovom periodu trudnoće fetus je najosjetljiviji na djelovanje različitih štetnih faktora, među kojima mogu biti i ljekovite tvari. Lijekovi mogu štetno djelovati na zametne stanice budućih roditelja i prije oplodnje. Ove promjene, shodno tome, mogu dovesti do naknadnog oštećenja potomstva. Tako štetno djeluju antitumorski lijekovi, imunosupresivi, neki antibiotici, psihotropni lijekovi. hormonalni lekovi struktura steroida. Zbog toga je preporučljivo suzdržati se od planiranja trudnoće 5-6 mjeseci nakon upotrebe takvih lijekova. Lijekovi mogu imati embriotoksično djelovanje, posebno u prve tri sedmice trudnoće, što se najčešće manifestira zaustavljanjem razvoja oplođene jajne stanice. Postoje i teratogeni efekti lijekova, koji dovode do različitih abnormalnosti fetalnog razvoja, a priroda defekta određena je trajanjem trudnoće, budući da je faza razvoja fetusa u trenutku izlaganja lijeku od velike važnosti. Teratogeni učinak lijekova ovisi o tome hemijska struktura, sposobnost prodiranja u placentu, doza lijeka, brzina njegove eliminacije iz tijela majke. Kombinacija određenih lijekova uzrokuje pojačane teratogene učinke. Uz istovremenu primjenu dva ili više lijekova koji imaju teratogeni učinak, rizik od razvoja urođenih defekata za fetus, shodno tome, značajno se povećava. Fetotoksični učinak očituje se u strukturnim i funkcionalnim abnormalnostima u razvoju fetusa i uzrokovan je značajnim negativnim djelovanjem na fetus. Uz različite komplikacije trudnoće (preeklampsija, bolest bubrega, itd.), lijekovi se mogu akumulirati u tijelu majke i stvoriti veće koncentracije u njenoj krvi i u tijelu fetusa, što pojačava njihov fetotoksični učinak. Da bi lijek djelovao na fetus, mora prodrijeti u njegov cirkulatorni sistem kroz placentu, koja je svojevrsna barijera koja štiti tijelo fetusa od štetnih faktora. Slijedom toga, u mnogim aspektima mogućnost štetnog djelovanja lijekova ovisi o stepenu ozbiljnosti funkcionalno stanje placentu i, posebno, njene manifestacije zaštitna funkcija. Kršenje ove funkcije najčešće se javlja s fetoplacentarnom insuficijencijom, koja se kao rezultat toga razvija razne bolesti i akušerske komplikacije. Zbog nesavršenosti metaboličkih i ekskretornih procesa fetusa, lijek i njegovi metaboliti mogu dugo ostati u tijelu fetusa. Na primjer, lijekovi koji smanjuju funkciju centralnog nervnog sistema, koje je uzimala trudnica, otkrivaju se u djetetovom tijelu mnogo dana nakon rođenja. Glavni procesi biotransformacije lijekova u tijelu fetusa odvijaju se u njegovoj jetri. U ovom slučaju u ovaj proces su uključene i nadbubrežne žlijezde, gušterača i gonade fetusa. Lijekovi se eliminiraju iz tijela fetusa metabolizmom u jetri; kroz bubrege sa urinom amnionska tečnost; povratni tok od fetusa do majke. Ako fetus izlučuje lijek kroz bubrege u amnionsku tekućinu, odatle lijek može ponovo doći do fetusa gutanjem. Zbog smanjene eliminacije iz fetusa, viši nivoi lijekova koji se daju majci prije rođenja mogu biti prisutni i kod novorođenčeta. Svi lijekovi se mogu podijeliti u pet grupa: grupa. Lijekovi koji u kontroliranim ispitivanjima na trudnicama nisu pokazali rizik za fetus u prvih 12 sedmica trudnoće i za koje ne postoje podaci o štetnom djelovanju na fetus u kasnoj trudnoći (većina multivitaminskih kompleksa, kalijum hlorid, suplementi gvožđa, trijodtironin). grupa. Kod djece čije su majke uzimale lijekove iz ove grupe (penicilinski antibiotici, heparin, inzulin, aspirin, metronidazol) nisu pronađeni lijekovi čije eksperimentalno ispitivanje nije pokazalo teratogeno djelovanje ili komplikacije uočene kod životinja. grupa. Prilikom testiranja ovih lijekova na životinjama otkriveno je njihovo teratogeno ili embriotoksično djelovanje. Nisu provedena nikakva kontrolirana ispitivanja ili nije proučavano djelovanje lijeka (izoniazid, fluorokinoloni, gentamicin, antidepresivi, antiparkinsonici). Ove lijekove treba propisivati samo kada je potencijalna korist veća od potencijalnog rizika. grupa. Primjena lijekova ove grupe povezana je sa određenim rizikom za fetus, ali je korist od njihove primjene veća od mogućih nuspojava (antikonvulzivi, doksiciklin, kanamicin, diklofenak). grupa. Dokazano je teratogeno dejstvo lekova iz ove grupe, njihova upotreba je kontraindikovana tokom trudnoće, kao i prilikom planiranja trudnoće (izotretionin, karbamazepin, streptomicin). Preporučljivo je da se trudnice suzdrže od uzimanja bilo kakvih lijekova u prvom tromjesečju trudnoće, osim ako lijekove nije izričito propisao ljekar, te da izbjegavaju sve druge lijekove osim onih koji odgovaraju prvoj grupi od gore navedenih. U slučajevima kada su bilo koji lijekovi korišteni uoči začeća ili u najranijim fazama trudnoće, tada prije svega lijek treba identificirati s gledišta njegovog mogućeg štetnog djelovanja. Ako se, na primjer, radi o vjerovatnom teratogenu, treba pokušati utvrditi odnos između vremena izlaganja i vjerovatnog vremena začeća. Ako se izlaganje poznatom teratogenu dogodilo u prvih 8 sedmica trudnoće, potrebno je dodatno istraživanje kako bi se razjasnio rizik moguća odstupanja u razvoju fetusa. Da biste to učinili, od 8 do 13 sedmica preporučljivo je odrediti nivo besplatnog β- hCG podjedinice, uraditi PAPP-A test od 8 do 11 sedmica, odrediti debljinu nuhalne translucencije (NT) ultrazvukom u 11-13 sedmici trudnoće. U tabeli ispod su navedeni lijekovi koje treba izbjegavati u ranoj trudnoći zbog njihovog štetnog djelovanja na fetus. 3. Mehanizmi
Do stvaranja defekata dolazi uglavnom u periodu embrionalne morfogeneze (3-10. nedelja trudnoće) kao rezultat poremećaja procesa reprodukcije, migracije, diferencijacije i smrti ćelije. Ovi procesi se odvijaju na intracelularnom, ekstracelularnom, tkivnom, međutkivnom, organskom i međuorganskom nivou. Oštećena reprodukcija ćelija objašnjava hipoplaziju i aplaziju organa. Poremećaj njihove migracije leži u osnovi heterotopija. Odgođena diferencijacija stanica uzrokuje nezrelost ili postojanost embrionalnih struktura, a njeno potpuno zaustavljanje uzrokuje aplaziju organa ili njegovog dijela. Povreda fiziološke smrti ćelije, kao i poremećaj adhezionih mehanizama ("lepljenje" i fuzija embrionalnih struktura), leže u osnovi mnogih distrofija (na primer, spina bifida). Eksperimentalna embriologija je dokazala da je teratogenetski terminski period, odnosno vremenski period tokom kojeg teratogeni agens može izazvati kongenitalnu malformaciju, od velikog značaja za nastanak razvojnih defekata. Ovaj period je različit za različite organe. Koristeći embriološke podatke, može se suditi o vremenu nastanka određenog razvojnog defekta i sastaviti teratološke kalendare za razvojne mane različitih organa. Formiranje malformacija također može biti zasnovano na zaustavljanju razvoja tokom kritičnog perioda, poremećaju procesa formiranja ili dizontogenezi i destrukciji tkiva. U ovom slučaju može doći do nerazvijenosti organa ili njihovih dijelova (hipogeneza) ili njihovog pretjeranog razvoja (hipergeneza), odsustva organa ili dijelova tijela (ageneza), ne ispravan položaj ili pomicanje organa, nepravilno formiranje jednog ili drugog tkiva (displazija). Postoje dvostruke (višestruke) malformacije, koje se temelje na abnormalnom razvoju dva ili više fetusa, i pojedinačne, povezane s kršenjem formiranja jednog organizma. Dvostruke malformacije, ili deformacije, su „nerazdvojeni“ blizanci, među kojima se, ovisno o području njihovog spajanja, razlikuju torakopagus, ksifopagus, pigopagus, itd. meko i tvrdo nepce, polidaktilija, urođene srčane mane. Prevencija razvojnih mana - antenatalni sistem fetalne zaštite. 4. Lijekovi koji se ne smiju koristiti u ranoj trudnoći
Lijekovi s visokim rizikom od izazivanja problema (za koje se zna da su teratogeni) ili izazivanja pobačaja. Varfarin - Brojni urođeni defekti. Dietilstilbestrol - Vaginalna adenoza i adenokarcinom kod kćeri. Androgeni - Virilizacija i brojne urođene mane. Antineoplastični agensi - Brojni urođeni defekti. Kortikosteroidi (visoke doze) - Rascjep nepca. Fibrinolitički lijekovi - abrupcija placente. Tetraciklini - žuta promena boje zuba, sporiji rast kostiju. Valproat - defekt neuralne cijevi. Analozi vitamina A - Brojni urođeni defekti u razvoju. Ciproteron acetat - Feminizacija muškog fetusa. Lijekovi s velikom vjerovatnoćom razvoja abnormalnosti (umjereno povećanje rizika). Amiodaron - Giht. Hlorokin - Gluvoća (nije otkazana za akutnu malariju). Litijum - Giht, defekti kardiovaskularnog sistema. Fenitoin - Brojne urođene mane (ne poništavati ako postoje apsolutne indikacije za potrebu kontrole epileptičkih napadaja). Drugi lijekovi koje treba izbjegavati. Antagonisti kalcija, grizeofulvin, omeprazol, kinolonski antibiotici, rifampicin, spironolakton, žive vakcine itd. - Teorijski rizik identifikovan u studijama na životinjama i drugim eksperimentalnim studijama. Primjena antikoagulansa u prvom tromjesečju trudnoće povezana je s nepovoljnim ishodom trudnoće u 35% slučajeva i opasna je za razvoj skeletnih abnormalnosti kod fetusa (posebno u 6-9 sedmici intrauterinog razvoja). Upotreba polnih steroidnih hormona povezana je sa povećanim rizikom od mrtvorođenosti, rađanja fetusa sa patologijom kardiovaskularnog sistema (tetralogija Fallot, transpozicija krvnih sudova), hipospadijom i razvojem neuroblastoma kod dece u adolescencija. Upotreba oralnih kontraceptiva u ranoj trudnoći povećava rizik od hromozomskih abnormalnosti i rizik od rađanja djece s Downovim sindromom za 2,8 puta. Rizik od razvoja neuroblastoma kod djece, posebno kod muškaraca, povećava se 1,2 puta. Može doći do blagog povećanja rizika od spontanog pobačaja u trudnoći koje se javlja tokom kontinuirane upotrebe oralnih kontraceptiva. Upotreba vitamina A u kritičnim periodima razvoja organa i sistema može dovesti do stvaranja višestrukih malformacija kod fetusa. Nijedan od tableta za smirenje ili tablete za spavanje nije potpuno bezbedno. Stoga, njihovu upotrebu, posebno u prvom tromjesečju, treba napustiti. U drugoj polovini trudnoće, lijekovi koji se koriste u pravilu više ne uzrokuju velike anatomske nedostatke. Neki lijekovi, iako nisu teratogeni, ipak mogu imati nuspojave na fetus kada se uzimaju u trećem trimestru trudnoće. U poslednjim nedeljama trudnoće ili tokom porođaja, lekovi uglavnom utiču na funkcije pojedinih organa ili enzimskih sistema novorođenčeta, a manje utiču na fetus. Kada se koristi u visokim dozama u poslednjim nedeljama trudnoće, acetilsalicilna kiselina može izazvati žuticu kod fetusa. Osim toga, po prijemu u prošle sedmice Prije porođaja, acetilsalicilna kiselina može uzrokovati poremećaj sistema zgrušavanja krvi tokom porođaja kod majke i izazvati krvarenje kod novorođenčeta. Aminoglikozidni antibiotici se u trudnoći mogu koristiti samo za apsolutne indikacije, jer štetno djeluju na slušni aparat i bubrege fetusa. Tetraciklini mogu uzrokovati hepatocelularnu nekrozu kod majke i poremećen razvoj kostiju i zuba kod fetusa. Levomicetin (kloramfenikol) može uzrokovati kolaps perifernih krvnih žila kod novorođenčeta ako se daje u neodgovarajućim dozama. Sindrom sijedu kosu uočeno kod novorođenčadi zbog majčinog liječenja hloramfenikolom, uzroci relativna kontraindikacija za upotrebu ovog lijeka u kasnoj trudnoći. Tiazidni diuretici (diuretici) mogu uzrokovati trombocitopeniju kod novorođenčadi, vjerovatno zbog direktnog toksičnog djelovanja na koštanu srž, i treba ih izbjegavati u kasnoj trudnoći. U tabeli su prikazani lijekovi koji se ne smiju koristiti u drugoj polovini trudnoće ili, u nekim slučajevima, s velikim oprezom. 5. Lijekovi koji se koriste tokom trudnoće
Prilikom propisivanja i odabira liječenja lijekovima u trudnoći treba voditi računa ne samo o njegovom pozitivne strane, ali i rizik za majku i fetus. Određeni lijekovi se mogu koristiti tokom trudnoće. Kada se folna kiselina prepisuje u količini od 400 mcg u prvom tromjesečju, smanjuje se rizik od razvoja defekata neuralne cijevi kod fetusa. Uobičajena dnevna doza folne kiseline za prevenciju anemije kod trudnica je 500 mcg. Upotreba multivitaminskih preparata 3 mjeseca prije trudnoće značajno smanjuje rizik od rađanja djece sa patologijama srca, krvnih žila i nervnog sistema (materna, elevit, vitrum-prenatal, gendevit). Međutim, teratogeni učinak može se primijetiti ne samo kod nedostatka, već i kod viška sadržaja vitamina u tijelu. Dakle, višak vitamina C može dovesti do hromozomskih abnormalnosti. Velike doze vitamina D mogu pomoći u uklanjanju kalcija iz fetalnih kostiju skeleta i smanjenju proizvodnje paratiroidnog hormona. Dakle, u nedostatku bilo kakvih bolesti ili komplikacija tokom trudnoće, jasno uravnotežena ishrana majke je sasvim dovoljna za njen normalan tok, pravilan razvoj i rast fetusa, te nema potrebe za propisivanjem multivitaminskih kompleksa, posebno u prvom tromjesečju trudnoće. Korisnije je jesti hranu bogatu vitaminima i mikroelementima, u skladu sa povećanim potrebama organizma. Za prevenciju i liječenje anemije kod trudnica najčešće se koriste preparati koji sadrže željezo i folnu kiselinu (fenuls, sorbifer durules, ferrum lek, maltofer, fero-foilgamma). Glavni zahtjev za takve lijekove je osigurati minimalnu dnevnu dozu željeza i folne kiseline (500 mcg). Moderni hormonski gestageni lijekovi (duphaston, utrozhestan) nemaju androgeni i anabolički učinak i nemaju virilizirajući učinak na fetus. Propisivanje glukokortikoidne terapije (metipred, deksametazon, prednizolon) bez indikacija da žena ima autoimune bolesti vezivno tkivo ili hiperandrogenizam nije opravdan zbog visokog rizika supresija nadbubrežne funkcije fetusa, razvoj osteoporoze i generalizacija infekcije. Antispazmodici (no-spa, papaverin) se koriste u prvom trimestru trudnoće. Preparati magnezijuma - Magne B6, Magnerot se mogu koristiti dugo vremena dok se ne eliminiše opasnost od pobačaja i tokom cele trudnoće za nadoknadu nedostatka magnezijuma. Treba ih uzimati s oprezom u slučaju arterijske hipotenzije. B-adrenergički agonisti (partusisten, ginipral, salgim) prodiru u fetus i doprinose povećanju nivoa glukoze i uzrokuju tahikardiju. Uz produženu upotrebu, novorođenčad imaju manifestacije slične dijabetičkoj fetopatiji. Najsigurniji antiemetički lijekovi su Cerucal i Raglan. Međutim, budući da se mučnina i povraćanje češće javljaju u ranoj trudnoći, važno je ograničiti upotrebu ovih antiemetici na minimum. Primjena antihistaminika (suprastin, pipolfen, cimetidin, ranitidin, tavegil) u prvom tromjesečju trudnoće, u pravilu, nije povezana s povećanim rizikom od razvoja kongenitalnih malformacija u fetusa. Antacidi (Almagel, Maalox) koji se koriste u drugom i trećem trimestru trudnoće takođe nemaju negativan uticaj za voće Laksativi koji su relativno sigurni za fetus su bisakodil i listovi sene. Međutim, ne preporučuje se česta i sistematska upotreba ovih lijekova. Primjena antibiotika tokom trudnoće treba biti strogo regulirana medicinske indikacije i sprovodi se pod nadzorom lekara. Relativno bezbedni i za majku i za fetus su: penicilin, ampicilin, amoksicilin, cefalosporini (cefazolin, cefotaksim, supraks), augmentin, vilprofen, eritromicin. Počevši od drugog tromjesečja trudnoće, mogu se koristiti antimikrobna sredstva za lokalno liječenje: terzhinan, Klion-D, miramistin, plivosept, klotrimazol. Rekombinantne interferonske pripravke (KIPferon, Viferon) preporučuje se primjena ne prije drugog tromjesečja trudnoće. U nekim slučajevima postoji potreba za korekcijom hipertireoze kod majke. U tom slučaju moguće je prepisati male doze karbimazola, metimazola ili propiltiouracila. Međutim, takvo liječenje može biti praćeno rizikom od hipotireoze i gihta kod fetusa (10%). Za hipotireozu se propisuju levotiroksin i kalijum jodid. U slučaju inzulinsko-zavisnog dijabetes melitusa, trudnicama se inzulin propisuje nakon konsultacije sa specijalistom i uz praćenje nivoa šećera u krvi. Heparin i heparini niske molekularne težine (fraksiparin) ne prolaze kroz placentu i nemaju štetne efekte na fetus. Dugotrajna (više od 6 mjeseci) primjena heparina u terapijskim dozama tokom trudnoće predisponira reverzibilnu osteoporozu i frakture. Fraxiparin ima niz prednosti: odsustvo hemoragijskih komplikacija kod majke i novorođenčadi i kliničkih znakova osteoporoza. Diuretici se ne smatraju potencijalno teratogenim za ljudski fetus, ali se ne može isključiti fetotoksični efekat diuretika različitih hemijskih grupa. Uz produženu primjenu velikih doza tiazida od strane trudnica, mogu se razviti hiponatremija i trombocitopatija kod novorođenčadi. Pod uticajem etakrinske kiseline uočava se slabljenje i gubitak sluha kod novorođenčadi. Furosemid nema negativan učinak na fetus. Lijekovi koji snižavaju krvni tlak (antihipertenzivi) mogu imati neželjeni učinak na fetus, povećavajući njegovu osjetljivost na efekte hipoksije. Kod novorođenčadi od majki koje su uzimale antihipertenzive, krvni pritisak je nešto niži tokom određenog vremenskog perioda nego kod zdrave dece. Tretman bronhijalna astma koristeći β- Adrenergični lijekovi (salbutamol) nisu kontraindicirani tokom trudnoće. Nuspojave lijekova koji se trenutno koriste za akutnu astmu (uključujući steroide i kromolin natrijum) nisu dokazani. Lijekovi koji se najčešće koriste tokom porođaja uključuju lijekove protiv bolova. Svi oni prolaze kroz placentnu barijeru, razlikuju se po brzini i količini prodiranja. Nijedan od narkotičnih analgetika koji se koriste (promedol, petedin, meperidin, dolantin, fentanil) ne može pružiti efikasno ublažavanje bolova bez izazivanja nuspojava za fetus. Najozbiljnija od njih je respiratorna depresija, koja je posebno izražena 2-3 sata nakon intramuskularne primjene ili unutar 1 sata nakon intravenske primjene ekvivalentnih doza. S tim u vezi, primjena ovih lijekova se prekida najkasnije 2 sata prije očekivanog trenutka rođenja djeteta. Sedativi ili sredstva za smirenje (fenotiazini, prometazin, promazin, propiomazin, hidroksizin), koji se koriste tokom porođaja za ublažavanje agitacije, često se koriste u kombinaciji sa narkotičkim analgeticima. Unatoč brzom prodiranju kroz placentnu barijeru i smanjenju srčane frekvencije fetusa, ovi lijekovi ne izazivaju depresiju kod novorođenčadi u preporučenim dozama. Diazepam (Valium, Seduxen, Relanium) uzrokuje tendenciju smanjenja krvni pritisak kod novorođenčeta i dugotrajnog poremećaja termoregulacije. Osim toga, novorođenče može doživjeti respiratornu depresiju. Epiduralna analgezija (u nedostatku relevantnih kontraindikacija) je sigurna metoda ublažavanja porođajnih bolova koja blagotvorno djeluje na fetus. Magnezijum sulfat može izazvati hipotenziju i letargiju kod novorođenčeta. odstupanje lijeka za trudnoću 6. Lista razvojnih mana
Ageneza pluća je urođeno odsustvo pluća uz glavni bronh sa aplazijom, patrljak glavnog bronha je očuvan. Rijedak razvojni defekt koji se može kombinirati s drugim urođenim anomalijama. Zdrava pluća rastu kompenzatorno, ispunjavajući skoro ceo grudni koš. Bilateralna renalna ageneza je fatalna anomalija u kojoj se oba bubrega ne razvijaju. Jednostrana bubrežna ageneza Akranija je deformitet izražen u potpunom ili djelomičnom odsustvu krova lobanje i odgovarajućeg kože. U teškim slučajevima akranije, mozak ima izgled rudimenta, koji se sastoji od vezivnog tkiva sa žilama i manjim ostacima moždanog tkiva, koji leži otvoreno (eksencefalija) na slabo razvijenoj, deformiranoj bazi lubanje; ponekad je mozak potpuno odsutan. Albinizam je urođeni nedostatak pigmenta u koži, kosi, šarenici i pigmentnim membranama oka. Postoje potpuni i djelomični albinizam. anencefalija - intrauterini defekt razvoj fetusa, koji se formira u ranim fazama trudnoće i obično je povezan s izlaganjem štetnim faktorima okoline, toksičnim tvarima ili infekcijama; gruba malformacija mozga - potpuno ili djelomično odsustvo moždanih hemisfera, kostiju svoda lubanje i mekih tkiva. Aplazija pluća. Atrezija jednjaka. Atresija jejunuma. Daunova bolest. Klub stopala. Rascjep nepca. Kongenitalna dislokacija kuka (displazija kuka). Kongenitalni kretenizam. Urođene srčane mane. Hidrocefalus je prekomjerno nakupljanje tekućine sadržane u šupljinama mozga i kičmenog kanala. Hidrocefalus može biti urođen ili stečen. Pojavljuje se kada je poremećena apsorpcija, prekomjerno stvaranje tekućine u šupljinama mozga i poteškoće u njenom odljevu, na primjer, kod tumora, adhezija nakon upalnog procesa. Hipoplazija pluća. Divertikule jednjaka su slijepo završavajući proces ili izbočenje organa. Divertikule se mogu nalaziti na granici sa ždrelom, na nivou bifurkacije (epibronhijalne), iznad dijafragme. Rascjep usne. Clubfoot. Kriptorhizam je stanje u kojem se jedan ili oba testisa ne pomjeraju u svoj pravilan položaj u skrotumu prije nego što se dječak rodi. Megakolon je razvojni defekt karakteriziran povećanjem ljudskog debelog crijeva. Etiološki faktor anomalije je urođena nezrelost inervacionog aparata debelog crijeva. Tok bolesti karakterizira zatvor od prvih godina, a ponekad i mjeseci života. Mikrocefalija je neurorazvojni poremećaj kod kojeg je obim glave osobe manji od dvije standardne devijacije od prosjeka starosti i spola. Mikrocefalija može biti kongenitalna (ponekad nasljedna) ili se javiti tokom prvih nekoliko godina života. Ovaj poremećaj može biti uzrokovan brojnim stanjima koja ometaju razvoj mozga. Često su uzrok sindromi povezani s hromozomskim abnormalnostima. Primarna mikrocefalija je uzrokovana gubitkom (delecijom) dvije kopije gena uz gubitak odgovarajuće funkcije koja kodira protein mikrocefalina. Nerazvijenost tibije i femura Omfalokela - (kila pupčane vrpce, pupčana kila, fetalna hernija) - vrsta urođenog defekta prednjeg trbušnog zida, u kojem se petlje crijeva, jetre i, ponekad, drugih organa šire izvan trbušne šupljine u hernialnoj vrećici. Omfalokela je uzrokovana defektom u razvoju mišića prednjeg trbušnog zida. Pilorična stenoza je kršenje pražnjenja želuca zbog suženja njegovog izlaznog dijela. Češće je uzrokovano cicatricijalnim suženjem duodenuma ulcerativne prirode neposredno ispod pylorusa, kao i suženjem antruma želuca ulceroznog ili tumorskog porijekla. Prava pilorična stenoza lokalizirana je u piloricnom kanalu i obično je uzrokovana ožiljnim ulkusom. Polidaktilija je anatomska devijacija koju karakterizira ì osoba ima više prstiju na rukama ili nogama nego inače. Suprotna devijacija je oligodaktilija. Polisomija na X hromozomu je povećanje grupe homolognih hromozoma zbog pojave redundantnih hromozoma (treći, četvrti itd. - respektivno, trisomija, tetrasomija itd.), P. se zasniva na pogrešnoj segregaciji hromozoma tokom anafaze ćelijska dioba Genitalni defekti Sindaktilija je urođeni defekt, genetska nasljedna bolest, koja se manifestira u potpunom ili nepotpunom srastanju prstiju na rukama i nogama kao rezultat njihovog neuspjeha da se odvoje tijekom embrionalnog razvoja. Prenosi se Y-vezanim nasljeđivanjem. Javlja se kod muškaraca. Jednostrana sindaktilija se opaža otprilike 2 puta češće nego bilateralna. Često u kombinaciji s drugim razvojnim nedostacima. Postoje jednostavni i složeni, potpuni i nepotpuni oblici sindaktilije. Moguće je da se nekoliko prstiju spoji u jedan konglomerat, a često su prisutne i amnionske trake. Klippel-Feil sindrom je rijetka kongenitalna malformacija vratnih i gornjih torakalnih pršljenova, koju karakterizira kratki i neaktivni vrat. Ova patologija je nasljedna i prenosi se autosomno dominantnim putem. Cri-cat sindrom se objašnjava parcijalnom monosomijom; nastaje kada dođe do delecije (sa gubitkom trećine do polovine, rjeđe potpunim gubitkom) kratkog kraka petog hromozoma. Za razvoj kliničku sliku sindroma, nije bitna veličina izgubljenog područja, već specifičan beznačajan fragment hromozoma. Povremeno se opaža mozaicizam zbog delecije ili formiranja prstenastog kromosoma-5. Shereshevsky-Turnerov sindrom je hromozomska bolest praćena karakterističnim abnormalnostima fizički razvoj, niskog rasta i seksualnog infantilizma. Monosomija na X hromozomu (XO). Spina bifida je kongenitalna anomalija u kojoj se jedan ili više kralježaka ne zatvaraju u području spinoznih procesa tokom intrauterinog razvoja, te prolapsiraju u preostali jaz. kičmena moždina sa školjkama. Fibrodisplazija je rijetka bolest (1 slučaj na 2.000.000), nastala kao posljedica mutacije ACVR1 gena, a manifestuje se urođenim razvojnim nedostacima – prvenstveno zakrivljenim nožnim prstima i poremećajima u vratnoj kičmi na nivou pršljenova od 2 do c7. Fetalni alkoholni sindrom (FAS) - kombinuje odstupanja u psihofizičkom razvoju djeteta koja se razlikuju po kombinaciji i težini, a uzrok je konzumacija alkohola žene prije i tokom trudnoće. Kiklopija je razvojni nedostatak kičmenjaka kod kojeg su očne jabučice potpuno ili djelomično spojene i smještene u jednoj orbiti koja se nalazi duž srednje linije lica. "Kiklopi" umiru u prvim danima života. Kranijalna hernija - razvojna anomalija, koja predstavlja izbočenje mozga i njegovih membrana kroz defekt kostiju lubanje Ekstrofija mokraćnog mjehura je urođena malformacija mjehura u kojoj se bešike Ispada da nije unutra, već spolja. Nedostaje prednji zid mokraćne bešike, kao i odgovarajući deo trbušnog zida, koji je rascepljen, pa je bešika otkrivena. Urin izlazi kroz otvore uretera. Postoji uretralna epispadija. Ektrodaktilija je urođena malformacija: nedostatak ili nerazvijenost jednog ili više prstiju i (ili) stopala. Može biti povezano sa odsustvom metakarpalnih i metatarzalnih kostiju Epispadi ì Ja sam rijetka složena malformacija genitourinarnog sistema čiji je glavni simptom rascjep prednjeg zida uretre i mokraćne bešike. Zaključak
Dakle, nema sumnje da su mnoge hemikalije, kao i neki lekovi, svakako teratogeni za ljude. Oni ne samo da mogu uzrokovati urođene defekte, već i ozbiljno poremetiti razvoj embrija u širem smislu. Čak i široko korišteni i odobreni lijekovi tokom trudnoće mogu uzrokovati razne komplikacije kod fetusa i novorođenčeta. Prilikom propisivanja bilo kakvog liječenja tokom trudnoće, treba imati na umu da se svi lijekovi propisuju samo prema indikacijama. Nijedan lijek nije apsolutno siguran i bezopasan. Bibliografija
1.E.I. Valkovich, E.A. Oleinik Trudnoća i teratogena dejstva lekova i niza hemijskih jedinjenja / Sankt Peterburg: 2012. 2.V.G. Klinička farmakologija Kukes / M.: GEOTAR-Media, 2008. .Sigurnost lijekova. Ekspresne informacije. Bilten br. 10, 1996. Međunarodna fondacija za efektivne i sigurnih lijekova. Ministarstvo zdravlja Ruske Federacije. Ruski univerzitet prijateljstva naroda. .Negativni efekti lijekova. Kombinovana upotreba droga. Interakcija lijekova i hrane: edukativni priručnik / Sastavio: V.A. Nikolaevsky, A.V. Buzlama - Voronjež: LOP VSU, 2006. - 99 str. .Raevsky P.M., Sherman A.L. Matematička obrada medicinskih i bioloških informacija. / P.M. Raevsky, A.L. Sherman Sat. M.: Nauka, 170 - 181 str. .Sigurnost lijekova. Ekspresne informacije. Bilten br. 10 1996. Međunarodna fondacija za efikasne i sigurne lijekove. Ministarstvo zdravlja Ruske Federacije. Ruski univerzitet prijateljstva naroda. .Curtis G. Trudnoća. Sedmica za sedmicom / G. Curtis (prevod s engleskog) - Sankt Peterburg: Izdavačka kuća "VES" - 2000. - 37 - 54 str.
Predavanje br. 4
Kongenitalne i nasljedne bolesti
I. Pojam kongenitalnih i nasljednih bolesti. Njihove razlike. Genokopije i fenokopije. Multifaktorske bolesti.
Kongenitalne bolesti – bolesti koje nastaju in utero (prenatalno), tokom porođaja (internacionalno) i postoje u trenutku rođenja.
Kongenitalne bolesti mogu biti nasljedne i nenasljedne, a češće su nenasljedne urođene bolesti.
Nasljedne bolesti– nužno su praćene oštećenjem genetskog aparata i naslijeđuju se.
Većina nasljednih bolesti javlja se odmah nakon rođenja i urođene su patologije.
Dakle, nisu sve urođene bolesti nasljedne i postoje neke nasljedne bolesti koje nisu urođene.
Fenokopija– nenasljedna promjena fenotipa organizma uzrokovana faktorima okoline i kopiranje manifestacije bilo koje poznate nasljedne promjene (bolesti). Uzrok fenokopije je poremećaj normalnog toka individualnog razvoja bez promjene genotipa.
Genokopija- pojava spolja sličnih fenotipskih osobina (bolesti) pod uticajem gena lociranih u raznim oblastima hromozomima ili u različitim hromozomima, tj. bolest je određena različitim genima. Na primjer, sljepoća može biti povezana s genetskim oštećenjem mrežnice i sočiva, koje kontroliraju različiti geni. Postoji nekoliko kopija gena Downovog sindroma.
Kongenitalna patologija, uzrokovan smetnjama u razvoju fetusa, javlja se kod otprilike 2% novorođenčadi i najčešći je uzrok neonatalnog mortaliteta i morbiditeta. Za većinu anomalija ne otkrivaju se hromozomske abnormalnosti, a one Ne su nasljedne.
Među nasljednim bolestima, bolesti sa nasljedna predispozicija (multifaktorska). Nasljedna predispozicija podrazumijeva da bolest nije striktno određena genetskim aparatom, već se nasljeđuju određena svojstva i karakteristike organizma, njegovih organa i sistema, što predisponira nastanku određenih bolesti (ateroskleroza, hipertenzija, dijabetes, tumori itd.). Multifaktorske bolesti se zasnivaju na poligensko nasljeđe, kada mnogi parovi gena zbroje svoj uticaj (aditivni efekat)
Osnovni koncepti genetike
Kariotip- skup hromozoma. Normalne ljudske ćelije imaju 46 hromozoma: 22 para autosoma (somatskih) i dva polna hromozoma, po jedan hromozom u svakom paru koji osoba dobija od svakog roditelja (46 XY - muški, 46 XX - ženski hromozomi su par X hromozoma). kod žena i X i Y hromozoma kod muškaraca.
Diploidni skup hromozoma u somatskim ćelijama (nastalim tokom mitoze).
Haploidni skup hromozoma u zametnim ćelijama - gametama (nastalim tokom mejoze).
Gene- dio DNK odgovoran za sintezu proteina. DNK (azotne baze (A, G, C, T), deoksiriboza i ostatak fosforne kiseline) je dvostruka spirala sa komplementarnošću. Triplet (kodon) – kodira sintezu 1 aminokiseline.
Genotip (kariotip)– skupovi karakteristika hromozomskog skupa pojedinca. Fenotip– skup manifestiranih znakova organizma tokom njegove interakcije sa okolinom.
Alele– kontrola alternativne opcije isti znak. Organizam koji ima dva identična alela jednog gena (BB ili BB) je homozigot, a različiti aleli (BB) su heterozigoti.
Nasljedna varijabilnost postoje dvije vrste. Kombinativno- miješanje nepromijenjenih gena. Mutacijski- promjena genotipa, sa naglim promjenama karakteristika.
Pleiotropizam gena- 1 gen je odgovoran za različiti znakovi(Marfanov sindrom kod Paganinija - arahnodaktilija, katarakta, abnormalnosti skeleta, srčane mane).
Penetrance- manifestacija, vjerovatnoća ispoljavanja osobine kodirane genom (učestalost kojom se abnormalni gen manifestuje klinički u obliku bolesti).
Ekspresivnost- stepen ispoljavanja znaka (stepen ekspresije kliničke manifestacije abnormalni gen kod različitih osoba).
Sibs- djeca istog roditeljskog para.
Proband– osoba preko koje je registrovana cijela porodica (obično podnosilac zahtjeva iz porodice koja se opisuje).
Nije sav genetski materijal lokaliziran na hromozomima. Postoji mitohondrijski genom (mtDNA) - mali kružni molekul, sadrži 13 gena, kodira sintezu citokrom oksidaza, ATPaza itd.
II. Teratogeni. Klasifikacija kongenitalnih bolesti u zavisnosti od perioda nastanka. Teratogeno dejstvo lekova.
Teratogeni faktori (ili teratogeni)- faktori koji uzrokuju malformacije (od grčkog teratos - deformitet).
Kongenitalne bolesti se dijele ovisno o tome od dana nastanka .
1) period progeneze odgovara sazrijevanju gameta (jajnih stanica i sperme) prije oplodnje (u tom periodu može doći do patologije gameta - gametopatije );
2) period cimatogeneze(iz grčkog kyema- embrion) odgovara periodu od oplodnje do rođenja. Period cimatogeneze se poklapa sa periodom cimatopatije . Razlikuje tri perioda:
· blastogeneza- period od oplodnje do 15. dana trudnoće. U tom periodu jaje se drobi i završava formiranjem embrioblasta i trofoblasta (u tom periodu dolazi do pojave blastopatije );
· embriogeneza- u periodu od 16. do 75. dana trudnoće dolazi do glavne organogeneze i formiranja amniona i horiona (u tom periodu dolazi do pojave embriopatije );
· fetogeneza- u periodu od 76. do 280. dana trudnoće dolazi do diferencijacije i sazrevanja fetalnih tkiva, formiranja placente, kao i rođenja fetusa (u tom periodu dolazi do pojave fetopatija ). Fetogeneza se, pak, dijeli na
· rani fetalni period (76-180 dana trudnoće) - moguća pojava bolesti rane fetogeneze ;
· kasni fetalni period (181-280 dana trudnoće) - moguća pojava bolesti kasne fetogeneze .
Tabela 4.1.
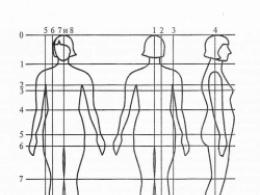
Kritični periodi ljudske embriogeneze, u sedmicama (Moore, 1973.)
| Podjela zigote, implantacija | Embrionalni period | Fetalni period | Porođaj | ||||||||
| 20-36 | |||||||||||
| Embrion obično umire u prisustvu teratogena | centralnog nervnog sistema | ||||||||||
| Srce | |||||||||||
| Gornji udovi | |||||||||||
| Oči | |||||||||||
| Donji udovi | |||||||||||
| Zubi | |||||||||||
| Čvrsto nebo | |||||||||||
| Spoljašnje genitalije | |||||||||||
| Uši | |||||||||||
Najviše proučavano uzroci cimatopatija su sljedeće:
jonizujuće zračenje: Pored direktnog dejstva na DNK i genetski aparat ćelije, jonizujuće zračenje ima i direktno toksično dejstvo na ćelije fetus u razvoju i uzrok je mnogih kongenitalnih anomalija kao rezultat izloženosti tokom trudnoće;
Teratogene virusne infekcije: virus rubeole je najmoćniji teratogen virus i uzrokuje veliki broj urođenih mana. Transplacentalna infekcija fetusa virusom u prvom tromjesečju trudnoće dovodi do razvoja velikog broja kongenitalnih anomalija. Virus rubeole remeti sintezu proteina u kulturama tkiva. Sindrom rubeole ujedinjuje trijada kongenitalnih anomalija : srčane mane, gluvoća i katarakta. Opisani su i slučajevi mikrocefalije, mentalne retardacije i mikrooftalmije. Teratogeno dejstvo drugih virusnih infekcija se raspravlja. Postoje izvještaji o teratogenim efektima virusa gripe, zaušnjaka (zaušnjaka) i varičele.
Teratogeno dejstvo lekova
Nemoguće je jednoznačno reći u kom periodu intrauterinog razvoja farmakoterapija može dovesti do ozbiljnijih posljedica. Najobimnije posljedice su obično oštećenja nastala u periodu blasto- i embriogeneze, iako u nekim slučajevima čak i poremećaji u periodu fetogeneze mogu biti nespojljivi sa životom. Istina, tijekom fetogeneze, za zaštitu fetusa, uključujući i ksenobiotske lijekove, dodatno zaštitna barijera– placenta.
Tokom trudnoće treba izbegavati uzimanje bilo koje vrste lekova kad god je to moguće, osim ako je neophodno da se spasi život majke ili fetusa. Ne postoje lijekovi koji se mogu smatrati potpuno sigurnim, posebno u ranoj trudnoći . Unatoč činjenici da su svi lijekovi koji se koriste testirani na trudnim životinjama, njihova sigurnost za ljude može se utvrditi tek nakon mnogo godina njihove upotrebe, kao što se dogodilo u SAD-u prilikom upotrebe. talidomid i dietilstilbestrol.
Rice. 4.1. Teratogeno dejstvo talidomida. Fokomelija kod novorođenčeta čija je majka uzimala talidomid tokom prva dva mjeseca trudnoće.
Talidomid je blagi sedativ koji se široko koristio u Europi 1960-ih sve dok se nisu pojavili epidemiološki dokazi da uzrokuje određene poremećaje u razvoju fetusa (fokomeliju) kada se koristi tijekom trudnoće. Kao rezultat poremećaji u razvoju udova Noge i ruke djeteta podsjećaju na morževe peraje - kratke batrljke udova smještene blizu tijela.
Dietilstilbestrol je sintetički estrogen koji se naširoko koristio 50-ih godina za liječenje prijetećeg pobačaja. Često su se razvijale kćeri žena koje su uzimale dietilstilbestrol epitelne abnormalnosti vagine, uključujući povećanje broja mukoznih žlijezda (vaginalna adenoza), u više teški slučajevi- bistrocelularni adenokarcinom.
Glavni uvjet za formiranje budućeg organizma je, prije svega, normalan bookmark i optimalan protok biosintetički (prvenstveno biosinteza proteina) procesi, reprodukcija ćelija; i kasnije prenatalni period- period fetogeneze - i normalno funkcionisanje formiranih organa.
Biosintetički procesi zahtijevaju Građevinski materijali(prvenstveno aminokiseline) i dovoljnu količinu energije ATP-a, za čiju proizvodnju su, pak, potrebni oksidacijski supstrati, kisik i enzimi (uključujući vitamine i mikroelemente).
Sve droge su opasne, zar ne? blokiraju biosintezu proteina (kao što je većina antibiotika), ili indirektno sprečavanje biosinteze (na primjer, glukokortikoidni lijekovi, koji ne samo da direktno blokiraju biosintezu mnogih proteina, već i pretvaraju glukogene aminokiseline u glukozu tokom glukoneogeneze i uskraćuju proces biosinteze glavnog građevinskog materijala).
Izuzetno opasne droge ograničavanje mitotičke aktivnosti ćelije (sve grupe antitumorskih lijekova, tzv. citostatika).
Biosintetski procesi će biti blokirani čak i ako ATP nedostatak - prilikom propisivanja lijekova koji blokiraju različite faze tkivno disanje, uključujući oksidacijske i fosforilacijske odspojivače (mnogi predstavnici gore navedenih kemoterapeutskih agenasa, tj. agenasa koji uništavaju strane subćelijske (viruse), ćelijske (bakterije, protozoe, tumorske ćelije), višećelijske (crvi), analoge ili lijekove hormona štitnjače , naprotiv, remeti sintezu ovih hormona).
Droge su opasne ometanje sinteze i implementacije efekata ne samo mnogi klasični, već i tzv. tkivni hormoni - prostaglandini, koji indirektno, putem mehanizama aktivacije enzima, učestvuju u procesima biosinteze proteina (nesteroidni protuupalni lijekovi), lijekovi protiv kalcija, supstance koje blokiraju djelovanje neurotransmitera (adreno-, holin-opijatni i histaminski receptori).
Lijekovi koji indirektno mogu poremetiti opskrbu fetusa aminokiselinama, vitaminima i glukozom sredstva za suzbijanje apetita (anoreksičari), koje žene ponekad uzimaju da izgube težinu, ili droge smanjenje apsorpcije navedena sredstva u gastrointestinalnog trakta majke (sorbenti, "crijevna" grupa antibiotika, sredstva koja pojačavaju peristaltiku ili slabe lučenje probavnih žlijezda ili žuči od strane jetre).
Pojava patologije fetusa s indirektnim djelovanjem (na tijelo majke) moguća je i zbog propisivanja svih lijekova koji na ovaj ili onaj način uzrokuju hipoksija (poremećena biooksidacija) - depresija respiratornog centra (opijati, "stem" tablete za spavanje), smanjenje cirkulacije placente - vazodilatatori i lekovi koji depresiraju srce usled pada sistemskog krvnog pritiska; ili, naprotiv, vazokonstriktori, koji izazivaju ishemiju posteljice sa očuvanim ili čak povišenim sistemskim krvnim pritiskom.
Lijekovi koji ometaju opskrbu fetusa su opasni glukoze (hipoglikemijski) ili blokira prijenos kisika hemoglobinom (tvorci methemoglobina kao što su antipiretici - derivati anilina).
Period blasto- i embriogeneze, kao što je već spomenuto, najranjiviji je i zbog toga što ne postoji placentna barijera, pa sve tvari iz krvi majke ulaze u budući organizam, bez obzira na njihovu hidro- i lipofilnost. Tokom fetogeneze, iz istih razloga, oni će biti opasniji lipofilna lijekovi. Vjerojatnost teratogenog djelovanja lijekova može se povećati kada se koristi zajedno s hepatotoksični lijekovi , budući da će biti poremećeni mehanizmi detoksikacije, na primjer, tzv. zaštitne sinteze i mikrosomalna oksidacija, čiji je cilj da se molekuli prenese hidrofilnost, što bi trebalo barem djelomično ograničiti prodor ovih lijekova kroz placentu.
III. Mehanizam nastanka patologije u fetusu kada trudnica puši.
nikotin, ugljen monoksid (CO) i druge toksične komponente duhanskog dima lako prodiru u placentu, smanjujući opskrbu fetusa kisikom, kao i utiču na strukturu i funkcioniranje pupčane vrpce i posteljice. Nikotin ima direktan uticaj na otkucaji srca. Efekti nikotina u u ovom slučaju zbog svog stimulativnog djelovanja na H-holinergičke receptore stanica medule nadbubrežne žlijezde, što stimulira oslobađanje kateholamina od strane potonje. Adrenalin i norepinefrin, stimulirajući b-adrenergičke receptore miokarda, doprinose povećanju snage i učestalosti srčanih kontrakcija (dakle aritmija), te stimulaciji a-adrenergičkih receptora žila pupčane vrpce i placente, kao i unutrašnje organe fetus ograničava protok krvi bogate kiseonikom u fetalna tkiva. Osim toga, stimulacija b-adrenergičkih receptora u masnom tkivu stimulira njegovu razgradnju, pa je moguć razvoj pothranjenosti fetusa.
ugljični monoksid (CO) ima veoma visok afinitet za hemoglobin (300 puta veći od O2), stoga je u stanju da se nepovratno veže za hemoglobin, formirajući kompleks koji nema sposobnost transporta i oslobađanja kiseonika - karboksihemoglobin (HbCO). Rezultat je hemička hipoksija.
Poznato je nekoliko komponenti duvanskog dima koje prolaze kroz placentu kancerogeni (npr. 5-benzpiren).
Kod trudnica koje puše:
- javljaju mnogo češće spontani pobačaji i komplikacije trudnoće i porođaja.
- veći rizik od ektopične (tubalne) trudnoće.
- Velika šansa prevremeni porod.
- 20-50% veći rizik od smrti fetusa i novorođenčadi.
- Pušenje kod majke može dovesti do predispozicije djeteta za respiratorne bolesti. Istraživanja su pokazala da je pušenje bilo kojeg roditelja tokom trudnoće povezano s većim rizikom od svih vrsta raka u djetinjstvu zajedno.
- pogoršanje ponašanja, intelektualnog i fizičke karakteristike budućeg deteta.
· novorođenčad majki pušača imaju „simptome odvikavanja od nikotina“.
IV. Mehanizam nastanka patologije u fetusu tokom alkoholizma trudnice.
Alkohol prolazi kroz placentu i ulazi u fetus. Štetno takođe alkohol (etanol) , i njegovi proizvodi razgradnje - na primjer, acetaldehid .
Alkohol može izazvati grč krvnih žila posteljice i pupčane vrpce, što dovodi do gladovanja fetusa kisikom.
acetaldehid:
· smanjuje nivo cinka u ćelijama ploda, što otežava njihov rast i razvoj;
· sposoban da izazove mutacije u DNK zametnih stanica, što može dovesti do ozbiljnih malformacija organa i tkiva fetusa.
Uz to, alkohol uzrokuje nedostatak vitamina i remeti metabolizam (hormoni, prostaglandini, itd.). Na kraju zahvaćeni su mnogi organi i sistemi fetusa, ali prije svega - centralni nervni sistem (uključujući intelekt i sferu ponašanja).
Konzumacija alkohola od strane žena tokom trudnoće značajno povećava rizik od pobačaja, male porođajne težine, mrtvorođenih, au najtežim slučajevima i razvoja fetalni alkoholni sindrom (FAS) ili sindrom alkoholne fetopatije. Ovo je naziv za fetalnu bolest uzrokovanu intrauterinim oštećenjem alkohola.
Za ovaj sindrom karakteristika kongenitalne anomalije srca, spoljašnjih genitalija, disfunkcija centralnog nervnog sistema, mala porođajna težina, poremećaji strukture kičme, uklj. spina bifida, zaostajanje djeteta u fizičkom i mentalnom razvoju.

Rice. 4.2. Dijete sa sindromom alkoholne fetopatije. Uočljive su karakteristične crte lica: mala glava, posebno lice, nisko čelo, nisko postavljene uši, uske oči, nerazvijena brada, specifičan nabor očnih kapaka, velika usta sa tankim usnama, konveksna gornja usna i uski crveni obrub („riblja usta“).
Posljedice oštećenja fetusa alkohola nepovratan i praktično neizlječiv.
Priroda posljedica izlaganja alkoholu na fetus ovisi o mnogim razlozima. Naravno, najvažniju ulogu igra količina alkoholnih pića i učestalost njihovog konzumiranja. Dnevni unos trudna 30 grama alkohola(ili druga alkoholna pića u smislu alkohola), u pratnji visok rizik od sindroma alkoholne fetopatije u nerođenom djetetu. Međutim, ovaj sindrom se često javlja kod djece čije su majke koristile 3-5 grama alkohol svakodnevno! Jedna sigurna doza za sve ne postoji, jer štetnost alkohola za fetus takođe zavisi od karakteristika žensko tijelo o preradi alkohola i reakciji na alkohol, stanju organa i sistema žene u vrijeme trudnoće, prirodi ishrane, povezanim lošim navikama, genotipu fetusa, trajanju trudnoće i mnogim drugim točkama.
V. Metode proučavanja nasljednih bolesti.
Klinička i genealoška metoda sastoji se u sastavljanju rodovnika s naknadnom analizom ispoljavanja osobine karakteristične za određenu nasljednu bolest u najvećem mogućem broju generacija srodnika pacijenta.
Znakovi nasljednih bolesti utvrđenih pedigreima su:
1) otkrivanje bolesti „vertikalno“: iz generacije u generaciju kontinuirano (sa dominantnim tipom nasljeđivanja) ili sa određenim prekidima (sa recesivnog tipa nasljeđe);
2) Mendelov odnos između broja bolesnih i zdravih braće (3:1; 1:1; 1:0);
3) veća učestalost bolesti kod srodnika nego kod nesrodnika.
Twin method sastoji se od poređenja intraparne podudarnosti (identiteta) monozigotnih i bratskih blizanaca koji žive u različitim i identičnim uslovima prema patološkoj osobini koja se analizira.
U prosjeku, na svakih 100 jednoplodnih porođaja dolazi jedan blizanac (višestruko rođenje); Štaviše, jednojajčani blizanci se rađaju rjeđe od bratskih blizanaca, otprilike 3-4 puta.
O nasljednoj prirodi patologije svjedoči visoka podudarnost za analiziranu osobinu jednojajčani blizanciživot u različitim uslovima, i obrnuto, niska konkordancija blizanaca, posebno onih koji žive u istim uslovima. Naprotiv, visoka podudarnost za bilo koju patološku osobinu jednojajčanih i bratskih blizanaca koji žive u istoj sredini jasno govori protiv nasljednog porijekla ove patologije i, naprotiv, potvrđuje odlučujući značaj egzogenih (spoljašnjih) faktora u njenom razvoju.
Statistička metoda stanovništva sastoji se od prikupljanja pedigrea među velikom grupom stanovništva, unutar regije ili cijele zemlje, u studiji genetski izolati . Izolirati je grupa ljudi, od 500 do nekoliko hiljada ljudi, koja živi izolovano od ostatka stanovništva zemlje. Genetski izolat karakteriše činjenica da se brakovi odvijaju samo unutar njegovih granica, uz visoku učestalost endogamnih brakova. Ovo na kraju dovodi do genetske izolacije od ostatka ljudi u zemlji. Kao rezultat, abnormalni recesivni geni se prenose iz heterozigotnih u homozigotne parove, što je praćeno povećanjem broja nasljednih bolesti.
citološka metoda - utvrđivanje genetskog pola ispitivanjem ćelija na prisustvo Barrovo telo. Kada ćelija ima dva X hromozoma (kao kod normalne žene), jedan od njih (Barovo tijelo) se inaktivira i kondenzira na nuklearnoj membrani. Odsustvo Barrovog tijela označava prisustvo samo jedan X hromozom(g normalan covek(XY) i sa Shershevsky-Turner sindromom (XO)). Barrova tijela se najlakše identificiraju u razmazima slojevitog epitela, koji se dobijaju struganjem bukalne sluznice.
Biohemijske i imunološke metode sastoji se od istraživanja biohemijski znaci, očigledno specifično za određene nasljedne bolesti. Na primjer, za dijagnosticiranje fenilpirogrožđane oligofrenije, fenilpirogrožđana kiselina se određuje u urinu; za dijagnozu anemije srpastih ćelija (S-hemoglobinoza), ispituje se prisustvo S-hemoglobina u krvi; za identifikaciju stanja imunodeficijencije, određuje se sadržaj različitih antitijela i populacija limfocita.
Dermatoglifska metoda– prepoznavanje nasljednih bolesti prema uzorku dlanova.

Rice. 4.3. Shematska ilustracija dlanovi zdravog djeteta (lijevo) i djeteta istog uzrasta sa Downovim sindromom.
Citogenetska metoda sastoji se od mikroskopskog pregleda strukture i broja hromozoma ćelija (leukocita, epitela itd.). Promjene u strukturi i broju hromozoma (hromozomske aberacije) znak su nasljedne prirode bolesti.

Rice. 4.4. Šematski prikaz ljudskih hromozoma (idiogram haploidnog skupa.

Rice. 4.5. Metafazna ploča sa jednostavnim bojenjem.
Molekularna genetika. Realizira se korištenjem Southern blot hibridizacije (uvođenje fluorescentne oznake - DNK sonde) i amplifikacije (povećanje broja kopija) sekcija DNK pomoću PCR (lančana reakcija polimeraze).
PCR se provodi u uzastopnim ciklusima. U svakom ciklusu dešavaju se sljedeći događaji:
- dvolančana DNK, kada se zagrije, dijeli se na svoje sastavne jednolančane lance i u tom stanju može poslužiti kao šablon za replikaciju;
- Jednolančani DNK lanci se zatim inkubiraju u prisustvu DNK polimeraze i rastvora koji sadrži mešavinu sva četiri nukleotida, kao i specifične sekvence DNK (prajmera), što dovodi do sinteze kopija dva molekula DNK.
Zatim se postupci ponavljaju ispočetka, i stari i novi jednolančani lanci se kopiraju kako bi formirali treću i četvrtu kopiju molekula DNK, zatim se sva četiri ponovo kopiraju i formira se osam molekula DNK, itd. broj raste geometrijska progresija. Kao rezultat 20-30 ciklusa, proizvodi se efektivna količina DNK. Jedan ciklus traje oko 5 minuta, a za molekularno kloniranje fragmenta DNK bez ćelija potrebno je samo nekoliko sati.
PCR metoda je vrlo osjetljiva: omogućava vam da otkrijete samo jedan molekul DNK prisutan u uzorku. Ista metoda je takođe pogodna za analizu sekvenci RNK u tragovima, za to se RNK prevodi u komplementarne DNK (cDNK) sekvence koristeći reverznu transkriptazu. Metoda se široko koristi u prenatalnoj dijagnostici nasljednih bolesti, otkrivanju virusnih infekcija, kao i u sudskoj medicini.
VI. Mutageni. Klasifikacija mutacija. Oznake usvojene za prikaz porodičnog stabla. Vrste nasljeđivanja defekata u genomu.
Mutacija– nagla promjena osobine zbog kvantitativnih ili kvalitativnih promjena u genotipu.
Mutageni– faktori koji uzrokuju mutacije.
Mutacije oni su :
· somatski (potencijalni razvoj tumora) nisu naslijeđene i stoga nisu nasljedne bolesti, iako utiču na genetski aparat ćelije ;
· gametičke (prenose naslijeđem).
§ Smrtonosno– praćene su smrću tijela u maternici, ili neposredno nakon rođenja.
§ Sublethal– smrt prije puberteta.
§ Hipogenitalni– u kombinaciji sa neplodnošću.
Po prirodi promjene genotip u skladu sa tri nivoa organizacije genetskog materijala (geni - hromozomi - genom) razlikovati mutacije – genski, hromozomski, genomski i citoplazmatski.
I. Genske mutacije povezan sa promjenama u strukturi pojedinih gena (dijelovi DNK koji kodiraju sintezu jednog proteina, jedne osobine).
· Monogena – mutacija u jednom genu sa promjenom jedne karakteristike (na primjer, albinizam, kratkoprsti); monogene mutacije uzrokuju prave nasljedne bolesti.
· Poligeničan – istovremene mutacije u različitim genima različitih hromozoma, koje izazivaju jednosmjerne promjene u tijelu koje određuju predispoziciju za određene bolesti (na primjer, ateroskleroza, hipertenzija, dijabetes melitus tipa II); nije naslijeđena sama bolest, već predispozicija za nju koja se ostvaruje pod uticajem određenih vanjski faktori. Bolest se razvija kako pod uticajem mutacija, tako i pod uticajem faktora sredine, tj multifaktorski . Čak i za istu bolest, relativna važnost naslijeđa i okoline u različite osobe možda neće biti isti.
· Poenta – oštećenje jednog nukleotida u genu, odnosno zamjena jedne aminokiseline u proteinu drugom (na primjer, fermentopatija, anemija srpastih stanica, gluhonemost).
II. Hromozomske mutacije- strukturna preuređivanja u pojedinačnim hromozomima: delecije, duplikacije, inverzije, translokacije.
· Brisanje je gubitak dijela hromozoma kao rezultat njegovog lomljenja. Većina delecija je smrtonosna zbog gubitka ogromnog dijela genetskog materijala. Brisanje kratkog kraka hromozoma 4 dovodi do razvoja Wolffovog sindroma; delecija kratkog kraka hromozoma 5 - Cri du chat sindrom - mjaukanje i slični zvukovi mačji plač tipične za ovu patologiju, često se uočavaju mentalna retardacija i srčane mane.
· Translokacija je prijenos odvojenog segmenta jednog hromozoma na drugi hromozom. At balansirana translokacija sav genetski materijal je očuvan i funkcionalno sposoban, tako da nema fenotipskih manifestacija. Takve osobe mogu razviti abnormalne gamete.
· Dupliciranje – udvostručavanje hromozomske regije.
· Inverzije – rotacija dijela hromozoma za 180 0.

Rice. 4.6. Shematska ilustracija razne vrste hromozomske mutacije.
III. Genomske mutacije- promjene u broju hromozoma u setu, koje nisu praćene promjenom njihove strukture . Broj hromozoma se mijenja više puta – formira se aneuploid skup hromozoma. Višestruka promjena u broju hromozoma ( poliploidija ) je nespojivo sa životom.
1. Monosomija – smanjenje broja hromozoma.
· Shereshevsky-Turnerov sindrom (disgeneza jajnika) - monozomija polnih hromozoma, javlja prilično često. Jedan X hromozom nedostaje (45, XO). U nekim slučajevima, drugi X hromozom je prisutan, ali se otkriva teška kršenja(izohromozom, parcijalna delecija, itd.). Gubitak drugog X hromozoma obično dovodi do smrti fetusa.
Preživjela djeca imaju limfedem vrata, koji je prisutan i kod odraslih, što dovodi do razvoja debelog vrata. Urođene srčane abnormalnosti, nizak rast, gojaznost i anomalije skeleta su česte. Intelekt nije oštećen. U prisustvu jednog X hromozoma (i odsustva Y hromozoma), primitivne gonade se razvijaju kao jajnici. Odsustvo drugog X hromozoma dovodi do poremećenog razvoja jajnika tokom puberteta. Jajnici ostaju mali i u njima se ne nalaze primordijalni folikuli. Poremećena je i sinteza estrogena, što se manifestuje poremećajem endometrijalnog ciklusa (amenoreja) i lošim razvojem ženskih sekundarnih polnih karakteristika. Dijagnoza se može postaviti u odsustvu Barrovih tijela u struganju bukalnog epitela kod osoba sa ženskim fenotipom ili analizom kariotipa.
· At autozomna monosomija ogromna količina genetskog materijala se gubi, pa je obično smrtonosna.
2. Triosomija – povećanje broja hromozoma za jedan.
· Klinefelterov sindrom (disgeneza testisa) - trizomija polnih hromozoma - javlja se prilično često. Manifestuje se prisustvom dodatnog X hromozoma (47, XXY rjeđe, pacijenti sa Klinefelterovim sindromom mogu imati dva ili više ekstra X hromozoma (48, XXXXY ili 49, XXXXY); Formira se muški fenotip.
Prije puberteta se ne primjećuju nikakve kliničke manifestacije. Dodatni X hromozom poremeti normalan razvoj testisa tokom puberteta nepoznatom metodom. Testisi ostaju mali i ne proizvode spermu, a pacijenti su obično neplodni. Nivo testosterona u krvi je nizak, što dovodi do poremećenog razvoja sekundarnih polnih karakteristika. Pacijenti imaju tendenciju da budu visoki (testosteron ubrzava okoštavanje epifize) i imaju eunuhoidni izgled sa visokim glasom, malim penisom i rastom dlačica ženski tip. Ponekad se primećuje i ginekomastija. Ponekad dolazi do smanjenja inteligencije. Dijagnoza Klinefelterovog sindroma može se postaviti pronalaskom Barrovih tijela u struganju bukalnog epitela kod osoba s muškim fenotipom ili analizom kariotipa.
· XXX sindrom ("superžene")- prisustvo trećeg X hromozoma kod žena. Većina pacijenata je normalna. Neki imaju poremećaje u mentalnom razvoju, smetnje menstrualnog ciklusa i smanjena plodnost (plodnost).
· XYY sindrom- prisustvo dodatnog Y hromozoma kod muškaraca. Većina pacijenata je normalna.
Neki mogu doživjeti agresivno ponašanje i blagu mentalnu retardaciju.
· Downov sindrom je najčešći autozomni poremećaj. Nastaje kao rezultat prisustva trećeg kromosoma 21, što dovodi do razvoja karakterističnih kliničkih manifestacija.
Djeca imaju karakterističan kosi oblik očiju spljoštenog profila, kosih očiju, izraženih vertikalnih kožnih nabora koji prekrivaju medijalni kantus, takozvanu sličnost sa licima Azijata, ranije nazvanih "mongoloid". Stalni simptom je mentalna retardacija. 30% pacijenata ima urođene srčane mane. Takođe, kod ovih pacijenata je povećana učestalost raznih infekcija, čira na dvanaestopalačnom crevu i akutne leukemije. Muškarci sa Daunovim sindromom su obično neplodni, ali žene mogu da rađaju decu. Potomstvo majki s Downovim sindromom može biti normalno jer ne sadrže sve gamete dodatni 21. hromozom.

Rice. 4.7. Djeca sa Downovim sindromom.
· Edwardsov sindrom- trisomija 18 hromozoma (47XX/XY, +18) je rijetka.
Klinički se manifestuje kao zaostajanje u fizičkom i mentalnom razvoju, praćeno karakterističnim fizičkim nedostacima kao što su „ljuljačka stopa“ i ruke stisnute u šake sa ukrštenim prstima. Kao rezultat teških lezija, djeca rijetko prežive duže od godinu dana.
· Patau sindrom- trisomija 13 hromozoma (47XX/XY, +13) je takođe retka. Većina djece umire odmah nakon rođenja.
Trizomiju 13 karakterizira poremećen razvoj subkortikalnih moždanih struktura (odsustvo olfaktornih lukovica, fuzija frontalnih režnjeva i jedne moždane komore) i struktura srednje linije lica (rascjep usne, rascjep nepca, nazalni defekti, jedno oko [kiklop]).
IV. Citoplazmatske (mitohondrijske) mutacije nastaju kao rezultat mutacija u plazmogenima koji se nalaze u ćelijskim organelama koje sadrže DNK - mitohondrijima. Neke patologije povezane s muškom neplodnošću povezane su s ovom vrstom mutacije. Neki tipovi bratimljenja mogu biti iz istih razloga, ali se nasljeđuju, po pravilu, samo po ženskoj liniji.
Standardni rodovnik koristi jednostavan simboli i pravila:
- Muškarci su uvek prikazani kao kvadrata, žene - u formi krugovima.
- Pacijent koji kontaktira genetičara radi izrade pedigrea - proband - označen je strelicom.
- Grafički prikazane veze između članova porodičnog stabla su samo tri tipa: “muževi-žene”, “djeca-roditelji” i “braća-sestre”.
- Supružnici, braća i sestre (uključujući rođake i rođake) uvijek su prikazani na istom horizontalnom nivou (tj. u istoj generaciji). Razlika u godinama nije bitna.
Zračenje i malformacije
Embrion 9 nedelja tokom vanmaterične trudnoće
Podaci o dejstvu jonizujućeg zračenja na ljudski embrion i fetus dobijeni su iz studija efekata terapije zračenjem (pri zračenju abdominalnog dela trudnica) i studija dece izložene intrauterinom zračenju u Hirošimi i Nagasakiju. Opšti zaključak ovih zapažanja je jasan - radiosenzitivnost fetusa je visoka, a što je fetus mlađi, to je veća.
Kod preživjele djece štetni efekti zračenja manifestiraju se u obliku različitih deformiteta, zakašnjenja fizičkog i mentalnog razvoja ili kombinacija istih. Najčešći deformiteti su mikrocefalija, hidrocefalus i abnormalnosti srca.
Malformacije i deformiteti koji su rezultat izlaganja zračenju in utero se zajednički nazivaju teratogenim efektima.
S jedne strane, mogu se smatrati stohastičkim efektima, imajući u vidu vjerovatnoću njihovog ispoljavanja i zavisnost od faze embriogeneze u kojoj je došlo do zračenja. Međutim, ispravnije ih je klasificirati kao vrstu somatskih efekata, jer se javljaju kod djeteta kao rezultat njegovog direktnog zračenja u stanju embrija ili fetusa. U svakom slučaju, teratogena dejstva ne treba mešati sa naslednim efektima koji se javljaju kod potomaka ozračenih roditelja koji nisu bili direktno izloženi zračenju.
Veza između teratogenog efekta i gestacijske dobi
Period najveće radiosenzitivnosti ljudskog embriona je vremenski znatno produžen. Vjerovatno počinje pri začeću i završava se otprilike 38 dana nakon implantacije; Tokom ovog perioda razvoja, rudimenti svih organa počinju da se formiraju u ljudskom embrionu kroz brzu diferencijaciju od primarnih tipova ćelija. Slične transformacije u ljudskom embrionu dešavaju se u svakom od tkiva između 18. i 38. dana. Budući da je prijelaz bilo koje stanice iz embrionalnog stanja u stanje zrelosti radiosenzitivniji period njenog formiranja i života (bez obzira da li se radi o neuro-, mio-, osteo- ili eritroblastu, itd.), sva tkiva na ovaj put se ispostavilo da je visoko radiosenzitivna.
Mozaičnost procesa diferencijacije embriona i povezana promjena u broju najosjetljivijih ćelija određuju stepen radioosjetljivosti određenog sistema ili organa i vjerovatnoću pojave određene anomalije u svakom trenutku. Stoga frakcionirano zračenje fetusa dovodi do ozbiljnijih oštećenja jer izloženost uključuje različite tipove zametnih stanica i njihovu različitu distribuciju, što uzrokuje oštećenje velikog broja primordija organa koji su u kritičnim fazama razvoja. Tokom ovog perioda, maksimalna šteta može biti uzrokovana vrlo malim dozama jonizujućeg zračenja; da dobijete anomalije u više kasni period embrionalni razvoj zahtijeva izlaganje velikim dozama.
Otprilike 40 dana nakon začeća teško je izazvati velike deformitete, a nakon rođenja nemoguće. Međutim, treba imati na umu da u svakom periodu razvoja ljudski embrion i fetus sadrže određen broj neuroblasta, koji su visoko radiosenzitivni, kao i pojedinačne zametne ćelije sposobne da akumuliraju efekte zračenja. Najveći rizik od razvoja mentalnih poremećaja je uočen kada je fetus izložen zračenju između 8 i 15 sedmica nakon začeća.
Embrion i fetus nakon zračenja
Telo embriona i fetusa ima izuzetno visoku radiosenzitivnost. Zračenje u ovom periodu, čak i u malim dozama (> 0,1 Gy), izaziva teratogene efekte u vidu različitih malformacija, mentalne retardacije i deformiteta. S jedne strane, oni se mogu smatrati stohastičkim efektima, što znači vjerovatnost njihovog ispoljavanja u zavisnosti od faze embriogeneze u kojoj je došlo do zračenja. Međutim, ispravnije ih je klasificirati kao vrstu somatskih efekata, jer se javljaju kod djeteta kao rezultat njegovog direktnog zračenja u stanju embrija ili fetusa. U svakom slučaju, teratogena dejstva ne treba mešati sa naslednim efektima koji se javljaju kod potomaka ozračenih roditelja koji nisu bili direktno izloženi zračenju.
Dostupni direktni podaci kod ljudi nedovoljni su za utvrđivanje maksimalne dozvoljene doze zračenja fetusa, pa je potrebno pribjeći ekstrapolaciji rezultata dobivenih u eksperimentima na životinjama na ljude. Radioembriološke studije na različite vrsteživotinje su provedene vrlo široko i pažljivo. Posebno su poznata klasična djela W. Russela, R. Rafa i I. A. Piontkovskog.
Starosno specifične reakcije na zračenje u embriogenezi
Izuzetno visoka radiosenzitivnost organizma u antenatalnom, intrauterinom periodu razvoja lako se objašnjava, budući da je u ovom trenutku to konglomerat dijeljenja i diferenciranja.